Ny metod kan ge bättre läkemedel – med hjälp av ljuskemi
En ny metod för att kontrollera funktionaliteten hos medicinska biomaterial har tagits fram genom att kombinera hydrolys och ljuskemi. I förlängningen kan resultaten leda till bättre mediciner och minskat beroende av djurförsök.
Den nya metoden har utvecklats av forskare vid Kungliga Tekniska högskolan, KTH, Karolinska Institutet, KI samt Uppsala universitet.
– Vi har fått fram en nyckel till att kunna kontrollera hur påkopplingen och frisläppandet av proteiner sker genom att kombinera fotokemi och hydrolys, säger KTH-forskaren Tove Kivijärvi.
För att kunna förbättra medicin genom design av material behöver man kunna kontrollera materialets funktioner på ett väldigt precist sätt. Då kan man skapa cellmiljöer som liknar människans redan i labbet, något som är viktigt för att kunna förstå sig på biologiska mekanismer, sjukdomsförlopp och hur kroppen reparerar sig själv. Biologiska material kan även användas för att studera hur läkemedel fungerar och för att kunna effektivisera läkemedelstestning och prekliniska studier.
– De flesta av dagens biomaterial bygger på teknologier som inte möjliggör den här nivån av kontroll av materialets funktioner och det är en av anledningarna till att det finns sådana enorma utmaningar inom vävnadsregenerering och avancerade terapier. Den här metoden som vi har utvecklat tar ett steg närmare den realiseringen, säger Tove Kivijärvi.
Skapade hydrogel
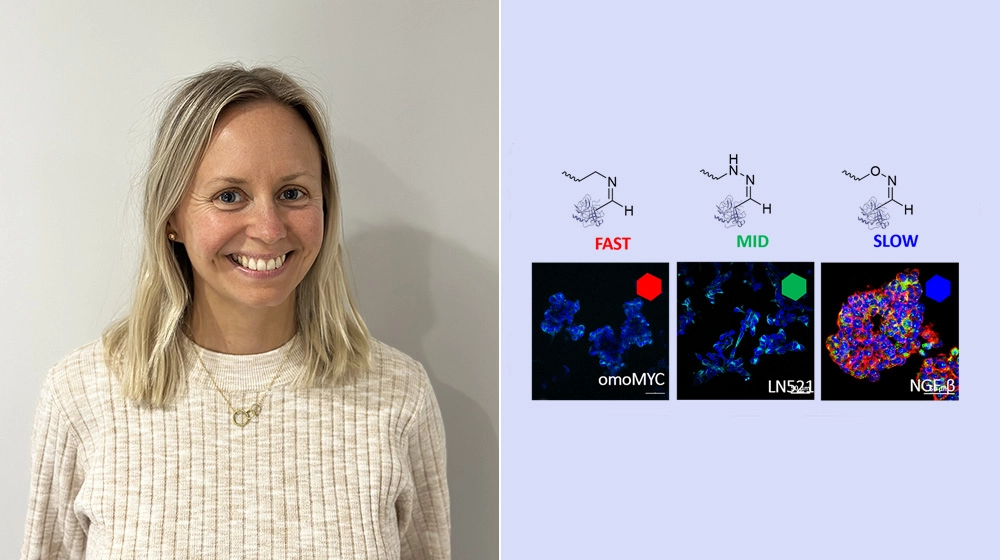
En studie publicerad i tidskriften Advanced Functional Materials beskriver Tove Kivijärvi och hennes medförfattare hur de har tagit fram en fotokemisk grupp som man har kopplat till en polymer. Av detta material har man sedan skapat en hydrogel. Genom att använda UV- eller NIR-ljus tillsammans med en serie hydrolys-benägna grupper kunde forskarna sedan kontrollera var och hur snabbt proteinerna frisläpptes i hydrogelen på ett mycket precist sätt.
– För att kunna möjliggöra den här typen av kontroll inom ett material kombinerade vi en av de mest fundamentala reaktionerna som finns, hydrolys, med reaktioner som kan styras helt av ljus. Kombinationen öppnar upp för möjligheter som tidigare inte fanns; att kunna reglera var och när en sådan fundamental reaktion sker. Det här är en viktig funktion när det kommer till att exempelvis frisätta proteiner för att påverka celler på förutbestämda sätt, säger Tove Kivijärvi.
Möjliggöra nya prekliniska studier
Beroende på vilket protein som forskarna inkluderade i materialet kunde de styra cellernas öde. Materialet kunde styra cellerna att fästa bättre vid ytan, vilket är viktigt för att cellerna ska kunna föröka sig och de kunde även styra cellerna att i stället differentieras mot mognare celltyper.
– Det största användningsområdet skulle vara mot precisionsmedicin. Att kunna ta ut celler från en patient och odla dem på det här materialet där vi vet var våra proteiner sitter, så att vi kan titta på hur cellerna responderar till proteiners verkan. Sedan kan vi studera hur olika läkemedel svarar mot patientens celltyp, säger Tove Kivijärvi.
Att kunna skapa cellmiljöer redan i labbet skulle ge verktygen som behövs för att kunna effektivisera, förbättra och möjliggöra helt nya prekliniska studier, tror forskarna bakom studien.
– Om vi kan utföra mycket mer precisa och säkra prekliniska studier kommer det att ge oss nycklarna till att förstå oss på komplexa underliggande sjukdomar och läkemedelsprocesser som vi annars inte harmöjlighet till. En annan viktig aspekt är att vi kommer att både kunna reducera och helt eliminera vissa djurförsök, säger Tove Kivijärvi.
Jon Lindhe ( jlindhe@kth.se )
